INTRODUCCIÓN
La enfermedad cardiaca es una causa frecuente de mortalidad y morbilidad en el paciente con diabetes mellitus (DM); la enfermedad arterial coronaria es la complicación cardiaca más frecuente de esta entidad(1-3). Se ha demostrado en las dos últimas décadas que los pacientes diabéticos normotensos y sin enfermedad arterial coronaria presentan con frecuencia disfunción ventricular izquierda, siendo la miocardiopatía diabética (CMD) o enfermedad muscular cardiaca diabética (EMCD) la entidad que justifica una mayor incidencia de fallo cardiaco congestivo en estos pacientes(4,5). Su patogenia se considera multifactorial y provoca cambios estructurales del miocardio que conllevan, en un primer estadio, a la disfunción ventricular izquierda (DDVI) y en fases posteriores la disfunción sistólica de ese ventrículo. La presencia de DDVI ha sido señalada como marcador precoz de la EMCD y su estudio ha despertado interés en los últimos años gracias a exploraciones no invasivas como la ecocardiografía Doppler (6-10).
La fibrosis y el depósito de colágeno que se produce en el corazón de estos pacientes cambian sus propiedades acústicas, cuya detección es posible a través de técnicas de caracterización tisular por ultrasonidos (CTUS). Julio Pérez y cols. han demostrado una disminución de la variación cíclica en el septum y pared posterior de pacientes diabéticos respecto a controles sanos, fundamentalmente pacientes con complicaciones microvasculares y descontrol metabólico. (11-12)
El presente estudio se propone caracterizar las propiedades acústicas del miocardio de pacientes diabéticos a través de técnicas de CTUS con el objetivo de detectar cambios muy precoces potencialmente indicativos de ECMD, así como correlacionarlos con la presencia de DDVI y comparar esta técnica con la de detección de disfunción ventricular por Doppler.
MÉTODOS
Se realizó un estudio transversal, prospectivo y controlado de 60 pacientes con diabetes mellitus (DM), que acudieron a la consulta de diabetes complicada del Hospital “Hermanos Ameijeiras” de La Habana, durante el período de un año .
Del total de pacientes diabéticos, 40 eran tipo 2 y 20 tipo 1 sin hipertensión arterial y con prueba ergométrica normal. Se excluyeron aquellos pacientes tratados con cualquier medicamento que pudiera deteriorar el control glucémico, así como a los portadores de ciertas condiciones clínicas (sepsis, neoplasias, alcoholismo).
Para su mejor estudio se dividieron en cuatro grupos:
Grupo 1: Pacientes con DM tipo 2 sin complicaciones microvasculares (20).
Grupo 2: Pacientes con DM tipo 2 con complicaciones microvasculares (20).
Grupo 3: Pacientes con DM tipo 1 con complicaciones microvasculares (20).
Grupo 4: Control, personas sanas (15).
Las complicaciones microvasculares evaluadas fueron:
Neuropatía somática de miembros inferiores: A través de estudios de neuroconducción motora y sensitiva a nivel del nervio peroneo y sural.
Neuropatía autonómica cardiovascular: Utilizando el software RITMOCARD versión 3.2 que analiza las vías de estimulación simpática y parasimpática del corazón a través del análisis de la variabilidad del intervalo R-R.
Neuropatía: Desde el estado de microalbuminuria persistente, determinadas por el método azul de Coomasie y con valores de positividad por encima de 30 mg/día, se confirmó en dos oportunidades y con un mes de intervalo.
Retinopatía: Proliferativa y no proliferativa, detectada por fundoscopía directa.
Se realizó un ecocardiograma bidimensional convencional que fue ejecutado en un equipo ALOKA PROSOUND 5500 y transductor multibanda de 2.5MHz con vistas ecocardiográficas estándar (eje paraesternal largo y corto, vistas de 2 y 4 cámaras). Con ecocardiograma en modo M desde las vistas paraesternales se obtuvieron los diámetros telediastólico (DTDVI) y telesistólico del ventrículo izquierdo (DTSVI), grosor del septum y pared posterior. La fracción ventricular (FE) izquierda fue calculada como índice de función sistólica.
La función diastólica se estudió realizando mensuraciones con Doppler pulsado de las velocidades de flujo transmitral, posicionando inicialmente el volumen muestra en el extremo distal de las valvas de la mitral desde la vista apical de cuatro cámaras. Se determinaron las siguientes variables: velocidad de pico diastólica temprana (onda E), velocidad pico diastólica tardía (onda A) medidas en cm/seg y fue determinada relación E/A. El tiempo de desaceleración de la onda E (TD) fue determinado desde el pico de la velocidad diastólica temprana hasta el punto en el cual la velocidad se extrapola a cero en la mesodiástole y fue determinado en milisegundos. Posicionando el volumen muestra parcialmente en el tracto de salida del ventrículo izquierdo fueron registradas simultáneamente la velocidad sistólica aórtica y diastólica mitral para determinar el tiempo de relajación isovolumétrica (TRIV) que fue medido en milisegundos también.
Se caracterizaron los siguientes patrones de disfunción diastólica (DD): Relajación prolongada : relación E/A <1, TD>240ms, TRIV>90ms; Pseudo normalizado: cuando la función diastólica continúa deteriorada existe esta fase de transición donde el flujo mitral por Doppler es aparentemente normal pero se necesitan dos métodos: maniobra de Valsalva y Doppler tisular para diferenciarlo de un patrón normal
Restrictivo: relación E/A >1, TD<160ms, TRIV>70ms.
El sistema de CTUS empleado fue el análisis de la retrodispersión integrada en septum y la pared posterior desde la vista paraesternal longitudinal utilizando el programa beta de manejo digital (DMS) del equipo, con la utilización de un transductor de 2.5 MHZ y el power Doppler. Se estudió la magnitud de variación cíclica (CVIBS), que es definida como la magnitud en decibelios (dB) de la variación del ciclo diástole-sístole y viene dada por el logaritmo de la razón entre la energía dispersada en diástole y la dispersada en sístole. Todas las determinaciones fueron realizadas por un mismo observador que desconocía las características clínicas de los pacientes.
Las variables cuantitativas se expresaron en media ± desviación estándar (SD). Para comparar los valores medios se utilizó la t-student cuando las asunciones de normalidad fueron satisfechas y cuando las desviaciones estándar fueron significativamente diferentes se utilizó la prueba de Wilcoxon como una alternativa paramétrica a la t-student.
Para analizar la relación entre las variables cuantitativas se utilizó un análisis de correlación lineal. El test de Chi-cuadrado se utilizó para determinar relación entre variables cualitativas. Se calculó un índice de variación cíclica para modo 2D, índice 2D: 0.36 septum+0.63 pared posterior, el criterio fue basado en escoger la combinación óptima de las variables pared posterior y septum de manera que el índice resultante diferenciara pacientes complicados de los no complicados. Se realizaron métodos de remuestreo para testar hipótesis de igualdad de las especificidades y sensibilidades de la variación cíclica con respecto a la función diastólica y la prueba de Long se utilizó para testar hipótesis de igualdad de áreas bajo la curva Roc de dos pruebas diferentes. Se tomó el valor de p<0.05 como indicador de significación estadística.
El diseño del estudio fue sometido a la aprobación del comité científico de la institución y se solicitó el consentimiento informado de todos los individuos incluidos en la investigación.
RESULTADOS
Se estudiaron 60 pacientes, 40 (66,6 %) presentaban DM tipo 2 y 20 (33,3 %) DM tipo 1; 38 (63,3 %) eran mujeres. Las edades estuvieron comprendidas entre 20 y 65 años con una media de (44,3 ± 9,6 años). El grupo control incluyó 15 voluntarios sanos, 9 (60 %) mujeres, con una media de edad (40 ± 4 años) y un rango entre 27 y 60 años. De los pacientes estudiados 40 (66,6 %) tenían complicaciones microvasculares.
Ecocardiograma bidimensional y Doppler:
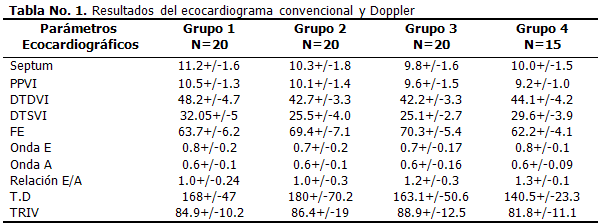
Todos los pacientes presentaron una adecuada función sistólica global ventricular izquierda con fracción de eyección media de (67,9 ± 6,9 %), las dimensiones internas del ventrículo izquierdo se mantuvieron dentro de los parámetros normales.
En los estudios Doppler realizados ninguno de los pacientes presentó regurgitación mitral ni otra valvulopatía. La media de la relación E/A en el estudio del flujo transmitral en los pacientes diabéticos mantuvo niveles más bajos que en el grupo control (1,11 ± 0,3 % vs. 1,3 ± 0,17 %; p<0.001) con diferencias estadísticamente significativas.
Los valores de onda E y onda A se comportaron de manera similar en todos los pacientes. El TRIV mostró una media de (86,75 ± 14,2 ms) sin diferencias significativas. El TD resultó más elevado en los pacientes diabéticos que en el grupo control (170,6 ± 56,4 vs. 140,5 ± 23,3 ms; p<0.04). (Tabla 1)
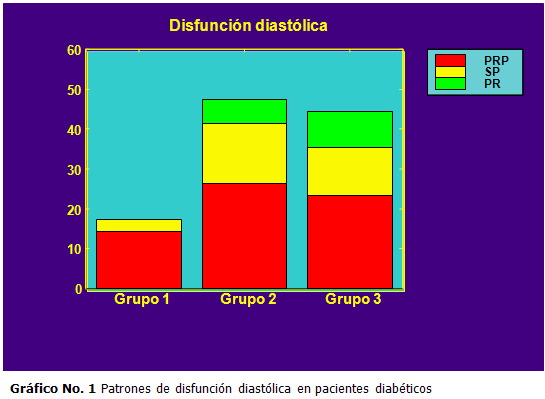
De los 60 pacientes estudiados 25 (42 %) presentaban disfunción diastólica; 4 (16 %) pertenecían al grupo 1; 11 (44 %) al grupo 2 y 10 (40 %) al grupo 3; hallazgos que muestran el mayor por ciento perteneciente al grupo de los pacientes complicados.
Se observó que de ellos, 15 (60 %) presentaron un patrón de relajación prolongada, 7 (28 %) pseudonormalizados y 3 (12 %) restrictivo. Resultó que en los grupos con complicaciones microvasculares aparecieron patrones restrictivos y mayores por cientos de pseudonormalizados indicando mayor grado de severidad de disfunción diastólica. (Gráfico 1)
Caracterización Tisular
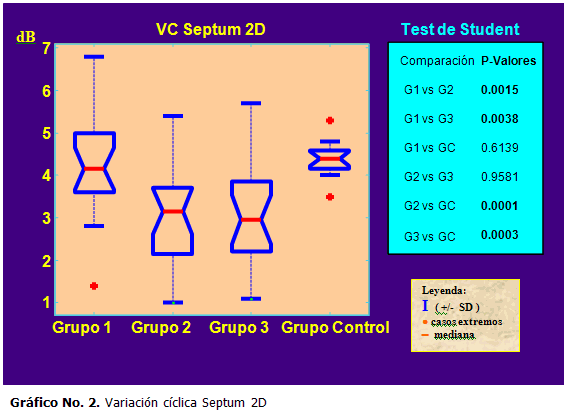
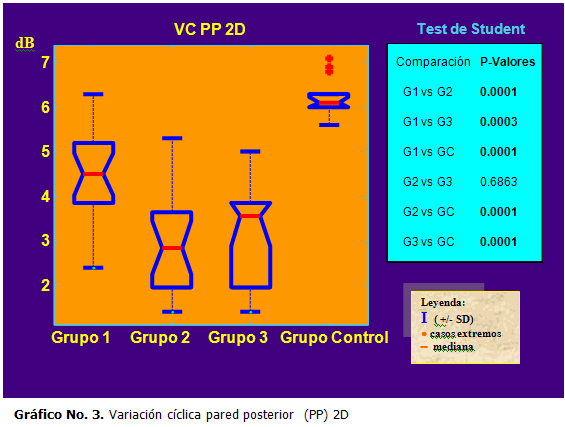
Se encontró una reducción de la variación cíclica a nivel del septum y la pared posterior en los pacientes con DM respecto al grupo control : septum 2D (3,4 ±1,3 vs. 4,4 ± 0,4 dB; p<0.003) y pared posterior 2D PP2D (3,4 ± 1,3 vs. 6,2 ± 0,4 dB; p< 0.000001). Los pacientes diabéticos con complicaciones microvasculares exhibieron valores más bajos de CVIBS que el resto de la población diabética, con diferencias estadísticamente significativas al compararlos con el grupo de pacientes no complicados (p<0.0001) en todos los casos a nivel del septum y pared posterior, en demostración de una importante correlación entre complicaciones microvasculares y alteraciones encontradas en el miocardio a través de CVIBS. (Gráficos 2 y 3)
Caracterización tisular y disfunción diastólica
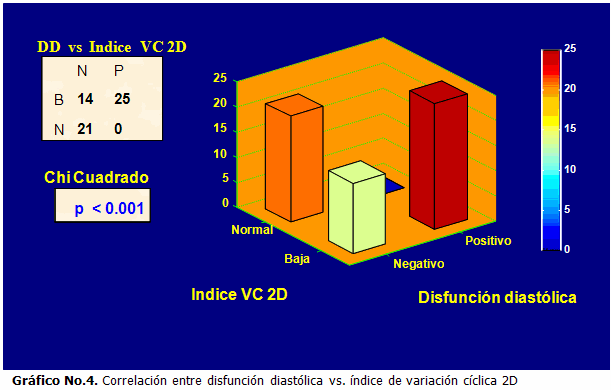
Cuando se analizó el grupo de pacientes que presentaban disfunción diastólica (25 pacientes) se obtuvo que en todos los casos los valores de magnitud de variación cíclica se encontraban alterados (100 %) y de 35 pacientes que no presentaban disfunción diastólica, 14 (23,3 %) tenían valores bajos de CVIBS mientras 21 (35 %) presentaban valores normales en 2D, resultando que existe una correlación estadísticamente significativa entre magnitudes bajas de CVIBS y la presencia de disfunción diastólica (p<0.001).
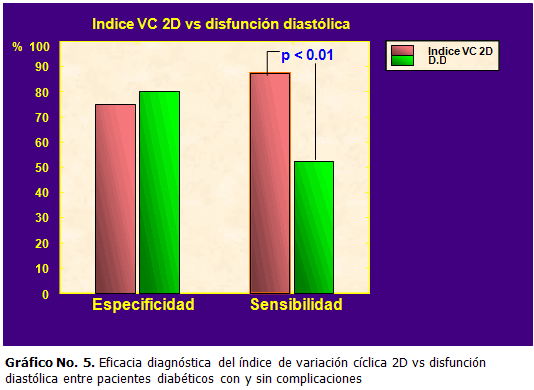
Al comparar ambas pruebas diagnósticas obtuvimos una mayor sensibilidad del índice de CVIBS comparando la disfunción diastólica en modo 2D (88 vs. 52 %; p<0.001), sin embargo la especificidad resultó similar con ambas técnicas. (Gráficos 4 y 5)
DISCUSIÓN
La existencia de una enfermedad muscular cardiaca diabética fue indicada por primera vez por Rubler en 1972 y este término fue introducido por Hamby y cols. en 1974.Evidencias posteriores que apoyan la existencia de esta entidad se obtienen de los resultados del estudio Framingham, donde se comprobó un aumento de la frecuencia de fallo cardiaco congestivo en diabéticos en ausencia de enfermedad arterial coronaria. (13-16)
La EMCD comprende varios elementos: macroangiopatía diabética, caracterizada por cambios bioquímicos y estructurales en la lámina media de las arterias coronarias extramurales; microangiopatía diabética, caracterizada por cambios histológicos en la pared de capilares y arteriolas intramurales pequeñas, microaneurismas y engrosamiento de la membrana basal capilar; cambios intersticiales en el miocardio con acumulación de tejido conectivo y glucoproteínas; presencia de neuropatía autonómica cardiaca y disfunción de células miocárdicas debido a desajustes metabólicos(17-19). Las anormalidades del llenado diastólico constituyen un signo temprano de disfunción ventricular izquierda y pueden preceder a las anormalidades de la función sistólica, que pueden ser explicados por anormalidades del llenado diastólico ventricular.(20-24)
La CTUS es una técnica diagnóstica basada en la aproximación a la definición de las propiedades estructurales y funcionales del tejido cardiaco, mediante el principio de que el estado físico del tejido puede expresarse de forma cuantitativa por el análisis de las interacciones entre ultrasonido y el tejido mismo. Julio Pérez y col. han planteado que diversos componentes estructurales del miocardio son determinantes de sus propiedades acústicas tanto en condiciones fisiológicas como patológicas y que la intensidad de reflexión dispersa va a depender del tamaño, forma y concentración de las diferentes estructuras reflectantes, de las diferencias de impedancia acústicas entre estas estructuras y el medio en que residen, así como su distribución espacial (11,12,25-28). El colágeno es el determinante principal tanto de la dispersión como de la atenuación del ultrasonido por el tejido miocárdico, al parecer por una sustancia de la que está compuesta, llamada hidroxiprolina(29). En nuestro estudio se encontró reducción de los valores de CVIBS en los pacientes diabéticos respecto a los controles a nivel del septum y la pared posterior; así como una correlación inversa entre valores bajos de CVIBS y complicaciones microvasculares coincidiendo con los resultados de estos citados autores. Este hallazgo sugiere que los pacientes complicados, aún en el período asintomático, pueden presentar afectaciones miocárdicas muy tempranas que podrían ser expresión de una EMCD en el futuro. Se ha señalado la disfunción diastólica como primer estadio de esta enfermedad, en nuestra investigación de 60 pacientes diabéticos estudiados 25 (41,6 %) presentaban DD y el mayor por ciento (84 %) pertenecían al grupo de pacientes complicados ; 60 % presentó un patrón de relajación prolongada. Con respecto a la relación E/A, considerada un indicador global de DD, encontramos diferencias significativas entre los pacientes diabéticos y el grupo control, con niveles superiores en este último, coincidiendo con la opinión de autores como Ángel Fernández, Poirier o Julio Pérez que consideran que estudiando dicha relación podríamos detectar cambios de la función diastólica en pacientes asintómaticos y con buena función ventricular sistólica (11,12,15,29-31). En nuestro estudio se le añade el hecho de presentar tiempos de desaceleración más prolongados en los diabéticos que en el grupo control, lo que es una evidencia más de las alteraciones de la función diastólica en este grupo de pacientes.
Al igual que Di Bello y cols (32-34) nuestra investigación demostró una menor sensibilidad del Doppler pulsado en la evolución de la disfunción diastólica global comparada con la caracterización tisular en pacientes asintomáticos. En cuanto a los segmentos analizados coincidimos con otros autores en que la pared posterior presenta una mayor sensibilidad respecto al septum cuando comparamos pacientes sanos con diabéticos; este comportamiento podría ser explicado sobre la base de que el depósito de colágeno es diferente en los diversos segmentos del miocardio y la pared posterior es más susceptible de ser afectada en fases muy precoces de la enfermedad extendiéndose después al septum en estadios más avanzados. (35-41)
La caracterización tisular está dejando de ser una técnica experimental para convertirse en una herramienta complementaria en los laboratorios de cardiología, de bajo costo comparada con estudios de medicina nuclear y de fácil acceso tanto para pacientes ambulatorios como para aquellos hospitalizados.(42-43)
Nuestra investigación constituye un acercamiento a uno de los objetivos más ambiciosos que persigue la cardiología de nuestros tiempos: identificar de forma no invasiva la estructura normal y las modificaciones patológicas que se producen en el tejido miocárdico detectando en este caso una entidad silenciosa y mortal como es la CMD en sus estadios más precoces.
CONCLUSIONES
Estos resultados indican que existe una reducción de la magnitud de la variación cíclica en septum y pared posterior en los pacientes diabéticos respecto al grupo control sano, siendo estas diferencias más significativas al analizar los pacientes complicados.
Se demostró además que existe una correlación entre la presencia de disfunción diastólica y valores bajos de variación cíclica, siendo la caracterización tisular una prueba más sensible que el Doppler pulsado para detectar anormalidades precoces del miocardio en pacientes diabéticos asintomáticos. El real significado de estos hallazgos se encuentra aún bajo un intenso debate, una de las hipótesis existentes podría ser la consideración de que estas alteraciones precoces del miocardio en pacientes diabéticos, sean un índice temprano de miocardiopatía diabética probablemente relacionadas con el depósito de colágeno.