INTRODUCCIÓN
La neumonía es la primera causa de mortalidad infantil en el mundo, y ocasiona la muerte de un niño menor de cinco años cada 15 segundos, es decir, dos millones cada año. Esta enfermedad representa el 20 % de los casi nueve millones de menores de cinco años que pierden la vida anualmente. Se estima que cada año 150 millones de niños y niñas desarrollan la enfermedad, y 11 millones son hospitalizados a causa de la neumonía, procedentes mayormente de países en desarrollo. Cerca de la mitad de las muertes podría evitarse a través de medidas de bajo costo (campañas de vacunación, diagnóstico efectivo y tratamiento empírico oportuno).(1,2)
El objetivo de este trabajo es exponer una guía de práctica médica, que sirva para abordar elementos sobre diagnóstico, epidemiología, etiología, factores de riesgos, clasificación y manejo del niño con neumonía adquirida en la comunidad.
DESARROLLO
Concepto
Las neumonías agudas infecciosas son procesos inflamatorios del parénquima pulmonar (alveolos e intersticio), reconocibles radiológicamente y evidenciados por una clínica dependiente de la edad, la constitución del paciente y, en parte, por la etiología que las origina.(3)
Epidemiología(4,5,6,7)
- Afecta a 450 millones de personas anualmente.
- Cada año, se producen 156 millones de nuevos episodios de neumonía en menores de cinco años.
- Responsable del 15 % de todas las defunciones de menores de cinco años. Se calcula que fue la causa de muerte en unos 922 000 niños en 2015.
- El 95 % de las neumonías adquiridas en la comunidad (NAC) ocurren en países en vías de desarrollo; como consecuencia, fallecen 2 millones de niños dichas naciones.
- El 8,7 % de estas neumonías son graves y constituyen una amenaza para la vida.
- El 90 % son de causa bacteriana, por Streptococcus pneumoniae y Haemophilus influenzae.
- En países desarrollados, representa solo el 3 % de las causas de muerte.
- En países en vía de desarrollo, representa el 19 % de las causas de muerte.
- En América Latina, representa el 14 % de las causas de muerte (estimado de 50 mil fallecidos).
- En Cuba, la tasa de mortalidad por neumonía en el menor de 5 años en 1970, era de 6 x mil nacidos vivos (23 % del total); en 2011, tasa de 0,3 x mil nacidos vivos (3 % del total); mostrando una reducción del 95 %.
Factores de riesgo
Los relacionados directamente con el niño, son:
- Sexo masculino.
- Menores de 5 años.
- Bajo peso al nacer.
- Desnutrición.
- Prácticas inadecuadas de lactancia materna.
- Déficit de micronutrientes (vitamina A, hierro y zinc).
- Enfermedades crónicas (cardiopatías congénitas, inmunodeficiencias congénitas o adquiridas, displasia broncopulmonar, anemia drepanocítica, desórdenes neuromusculares y asma bronquial).
- Ingresos por insuficiencia respiratoria aguda (IRA).
- Uso previo e indiscriminado de antimicrobianos.
- Falta de inmunizaciones.
Los relacionados con el medio socio- ambiental:(8,9,10,11,12)
- Exposición al humo u otros contaminantes, enfriamiento.
- Hacinamiento.
- Contaminantes domésticos.
- Asistencia a círculos infantiles, guarderías o casas de cuidadores.
- Falta de percepción del riesgo por parte del personal de salud.
- Atención médica tardía.
- Bajo nivel de escolaridad de la madre.
- Edad materna.
Clasificación(13)
Las neumonías pueden clasificarse desde varios puntos de vista. Las dos más importantes en el orden práctico, son las siguientes:
Según la expresión clínica y radiológica (clasificación anatomo-clínica):
1. Condensante:
- Lobar o segmentaria: Expresión clínica de Síndrome de Condensación; y radiológicamente, radiopacidad que afecta lóbulos o segmentos pulmonares (puede ser redondeada).
- A focos diseminados (bronconeumonía): Expresión clínica de Síndrome de Infección Respiratoria Baja y engrosamiento hiliar, más radiopacidades difusas en el estudio radiológico de tórax.
2. Intersticial:
Expresión clínica de Síndrome de Obstrucción Bronquial Difuso; y radiológicamente, evidencia de lesiones lineales hilio fugales, opacidades parahiliares, y en ocasiones atrapamiento de aire.
Según su origen o lugar de adquisición:
- NAC: Se presenta en niños que no han estado hospitalizados por lo menos de 7-10 días antes, o con síntomas después de 48 horas del egreso hospitalario, y que tengan una evolución menor de 15 días.
Etiología
En la infancia, la mayor frecuencia corresponde a las neumonías producidas por microorganismos (bacterias y virus); su comprobación es difícil por cultivo. Los virus son los agentes más frecuentes de neumonías en niños entre dos meses y cuatro años de edad, pero puede producirse una coinfección con bacterias o una infección secundaria bacteriana. A partir de los cinco años, la etiología bacteriana es más frecuente.(14,15,16,17)
Las neumonías condensantes deben ser consideradas de etiología bacteriana con fines terapéuticos.
Los principales agentes causales de neumonías en las distintas edades son:
- En los neonatos, la neumonía no es clasificable como NAC, y en general su tratamiento es el mismo que se recomienda para sepsis neonatal, que cubre todos los gérmenes, incluyendo enterobacterias (Streptococcus del grupo B +++, Escherichia coli +++, otros Gram negativos ++, Lysteria monocytogenes +, Staphylococcus aureus, Ureaplasma urealyticum +, citomegalovirus (CMV) +, enterovirus + y el virus sincitial respiratorio (VSR)).[1]
- Los niños de tres semanas a tres meses de nacidos, son los de mayor dificultad diagnóstica, hecho que genera mayores dudas con respecto a la terapéutica idónea. Los virus tienen una alta incidencia en esta edad como causantes de procesos respiratorios, y por su estado inmunológico poco efectivo tienen más riesgo de sobreinfectarse con patógenos como Streptococcus pneumoniae, Haemophilus influenzae tipo b (Hib), S. aureus y Klebsiella pneumoniae. Mientras más pequeños son los niños de este grupo, más probabilidad tienen de que la causa sea viral, pero también más riesgo hay de que evolucione en forma tórpida, y se presente la coinfección bacteriana, lo que obliga a un seguimiento estricto de su evolución. (Streptococcus pneumoniae +++, Chlamydia trachomatis +, Haemophilus influenzae b +, Ureaplasma urealyticum, L. monocytogenes, Bordetella pertussis, Staphylococcus aureus, VRS +++, CMV +, Parainfluenza, ADV y PI +.)
- En el grupo de cuatro meses a cinco años, los agentes de mayor incidencia son las bacterias como S. pneumoniae, y ocasionalmente VSR. En poblaciones no vacunadas (por acceso reducido a la atención) sigue predominando el Hib. En menores de 6 meses con neumonía afebril, antecedentes de conjuntivitis (50 % de los casos), de nacimiento por el canal del parto, expresión clínica de obstrucción bronquial y afección sistémica, debe sospecharse como causa principal la Chlamydia trachomatis. (Streptococcus pneumoniae +++, Haemophilus influenzae b++, Mycoplasma pneumoniae ++, Staphylococcus aureus +, VRS ++++, PI +++, influenza ++, ADV ++.)
- En niños de cinco a diez años el germen de mayor prevalencia es el neumococo, secundado por el Mycoplasma pneumoniae, sobre todo en mayores de 8-9 años. (Streptococcus pneumoniae ++++, Mycoplasma pneumoniae ++++, Chlamydia pneumoniae +, Staphylococcus aureus +, Streptococcus Grupo A +, virus: influenza +++, ADV, PI, VRS +.)
- Niños de más de diez años (Mycoplasma pneumoniae ++++, Streptococcus pneumoniae ++++, Influenza ++, otros virus respiratorios +, Mycobacterias +, Staphylococcus aureus +, Legionella pneumophilla +, Streptococcus A +, Chlamydia pneumoniae +).
En nuestro medio el neumococo representa la causa más frecuente de neumonía infecciosa bacteriana, desde los tres meses y hasta los 18 años de edad. La coinfección pneumococo-micoplasma afecta al 15-20% de los casos. A partir del año 2000, el estafilococo aureus resistente a metilpenicilina (MRSA), ha sido observado en neumonías graves y rápidamente progresivas.(11,13,14)
Cuadro clínico
Las manifestaciones clínicas de la neumonía varían según la edad, extensión de la enfermedad y agente etiológico. El cuadro clínico del lactante se caracteriza por síntomas generales como fiebre, rechazo alimentario, decaimiento, irritabilidad y palidez. Los signos respiratorios incluyen aleteo nasal, taquipnea >50/min, quejido, retracción de músculos intercostales, tos y cianosis, en los casos graves. En la auscultación puede existir disminución del murmullo vesicular pulmonar, crepitaciones finas, broncofonía y respiración soplante.(18,19)
Un grupo especial de alto riesgo son los menores de tres meses, cuyos síntomas y signos son menos específicos que en niños mayores. La fiebre no siempre está presente, y en casos graves la infección puede manifestarse como hipotermia. El compromiso del estado general puede ser tan sutil como la percepción de la madre de que el niño "no está bien". La presencia de tos debe ser investigada como posible infección respiratoria aguda baja en todo menor de tres meses.
En el preescolar y escolar los síntomas son similares a los de los adultos, incluyendo fiebre alta, escalofríos, cefalea, decaimiento y vómitos. Los signos destacados son tos con expectoración, dolor torácico localizado o referido al abdomen en neumonías basales. La auscultación se caracteriza por disminución del murmullo vesicular, crepitaciones finas, broncofonía y respiración soplante. Además, existe matidez y aumento de vibraciones vocales. Pueden presentarse también como un síndrome febril sin foco clínico evidente, con ausencia de signos respiratorios iniciales, y diagnosticarse solo por una radiografía de tórax.(3,20,21)
Clásicamente se han descrito dos formas clínicas de neumonía: la típica (fiebre, escalofríos, dolor costal y tos productiva) referida principalmente a la etiología neumocócica y la atípica (comienzo gradual, tos no productiva, cefalea, malestar general, etc.) causada preferentemente por virus o agentes bacterianos intracelulares (Mycoplasmas y Chlamydophilas). Esta distinción es aplicable a niños mayores y adolescentes, pero en neonatos y lactantes se hace más difícil.
- Neumonía típica (condensante):
Síndrome de condensación inflamatorio: Comienzo abrupto, generalmente precedida de un cuadro catarral, con polipnea (frecuencia respiratoria más de 50 respiraciones por minuto en niños menores de un año de edad, y más de 40 en niños mayores), tiraje, disminución de la expansibilidad torácica, aumento de las vibraciones vocales al llanto, o la voz cuchicheada en la zona afectada, matidez en dicha zona y disminución del murmullo vesicular, con la presencia de estertores húmedos, broncofonía, respiración soplante o soplo tubárico.
Síndrome de IRA baja: Más común en niños pequeños menores de dos años, donde la condensación puede presentarse a focos diseminados (bronconeumonía): Polipnea, tiraje, estertores húmedos finos diseminados en ambos campos pulmonares.
- Neumonía atípica (intersticial):
Comienzo gradual, fiebre, tos no productiva, cefalea, malestar general y expresión clínica del Síndrome de Obstrucción Bronquial Difuso con polipnea, tiraje, espiración prolongada, hipersonoridad pulmonar, disminución del murmullo vesicular con estertores húmedos finos y sibilancias.
Las Guías Prácticas de la Organización Panamericana de la Salud del año 2009 recomiendan, para cuando no sea posible contar con radiografía de tórax, considerar según el cuadro clínico: neumonías, neumonías graves y neumonías muy graves. (Cuadro 1).(22)
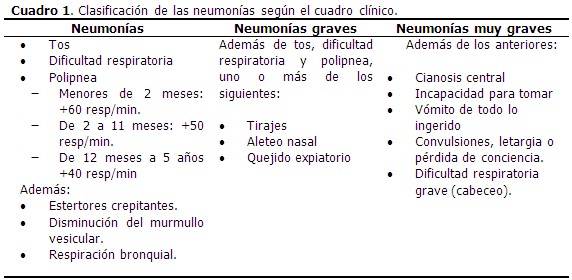
Diagnóstico
Se realiza con el cuadro clínico y se confirma con la radiología. La Organización Mundial de la Salud (OMS) recomienda la evaluación de la frecuencia respiratoria, ya que en el 85 % de los niños con neumonía se presenta como un indicador temprano y fácil de observar. La presencia de tiraje subcostal, cianosis, dificultad para alimentarse y somnolencia, son indicadores de severidad del cuadro. Deben considerarse signos y síntomas predictivos con vistas a indicar un Rx de tórax, sobre todo en niños pequeños: fiebre alta mantenida o fiebre que reaparece en una IRA, dolor torácico o abdominal, estertores crepitantes focalizados, falta de aire que se incrementa, tos persistente con fiebre.
La radiología confirma el diagnóstico, su localización y forma anatomoclínica; detecta complicaciones, pero no se relaciona directamente con la etiología del cuadro, en niños con evolución clínico-humoral satisfactoria sin complicaciones iniciales. No es imprescindible repetirla para dar el alta.(23,24,25)
Dentro de la analítica general podrían ser de utilidad el leucograma con diferencial, en las neumonías bacterianas típicas suelen presentar leucocitosis de mayores de 12 x 106/µl, con aumento, en la población leucocitaria, de polimorfonucleares mayor del 60 %, y desviación a la izquierda (más de tres stabs), con presencia de granulaciones tóxicas. La velocidad de sedimentación globular (eritrosedimentación) se eleva generalmente en las neumonías bacterianas, al igual que la proteína C reactiva.
Los exámenes microbiológicos tienen muy poca positividad y no se usan en la atención primaria de salud (APS). A nivel hospitalario, es importante indicar hemocultivo en niños con diagnóstico de neumonía bacteriana.(26)
Debe realizarse cultivo del líquido pleural en casos complicados con derrames paraneumónicos.(27) Donde existan posibilidades o ante un interés epidemiológico, se debe realizar estudio de secreciones faríngeas profundas para el diagnóstico virológico y de bacterias atípicas.
Complicaciones
Las complicaciones son más frecuentes en niños con riesgo. Se sospechan cuando la evolución es tórpida, persiste la fiebre y aparecen signos y síntomas nuevos. Dependen de factores relacionados con el niño enfermo, el agente causal y el medio ambiente donde este se desarrolla, el mismo donde adquirió la afección. Se incrementa el riesgo de complicaciones en lactantes pequeños y niños nacidos con bajo peso al nacer o pre términos, y pacientes portadores de comorbilidades. Los gérmenes resistentes a los antibacterianos o los muy virulentos, que condicionan una rápida evolución de la neumonía, ocasionan complicaciones más comúnmente.(28,29,30) Las más frecuentes complicaciones de las neumonías se clasifican en intratorácicas y extratorácicas:
Intratorácicas: 1) Respiratorias: Derrame pleural, absceso pulmonar, atelectasia, neumatoceles, pioneumotórax, fístulas broncopleurales, bronquiectasias, edema pulmonar; 2) No respiratorias: Insuficiencia cardíaca, miocarditis, pericarditis, mediastinitis, adenopatías mediastinales.
Extratorácicas: Íleo paralítico, shock, sepsis, desequilibrios hidrominerales, otitis media aguda, sinusitis, focos sépticos a distancia (artritis, meningitis).
Criterios de ingreso hospitalario
- Niño menor de un año.
- Niños mayores de un año con:
- Cuadro radiológico de neumonía extensa (imagen radiológica que sugiera afectación de uno o más lóbulos pulmonares).
- No respuesta al tratamiento de primera línea a las 72 horas de iniciado (empeoramiento clínico y/o radiológico).
- Presencia de factores de riesgo biológicos y sociales.
- Neumonías extensas o complicadas.
- Pacientes con dificultad respiratoria.
Tratamiento
Ambulatorio: Los niños mayores sin riesgos, con neumonías limitadas, no complicadas y condiciones en el hogar, pueden ser tratados ambulatoriamente con el correspondiente seguimiento por el área de salud.
Medidas generales:
- Vigilancia de la evolución clínica en las primeras 48-72 horas.
- Orientación sobre las medidas de higiene personal y ambiental para evitar la propagación de la enfermedad (aseo diario, lavado de manos, aislamiento).
- Alimentación adecuada según las necesidades.
- No suspender la lactancia materna.
- Ofrecer líquidos, no forzar alimentación sólida. Se sugiere fraccionar los alimentos (menos cantidad y mayor frecuencia).
- Tratamiento para la fiebre: paracetamol (10-15 mg/kg dosis cada 4-6 horas), ibuprofeno (5-10 mg/kg dosis cada 6-8 horas), o dipirona (20 mg/kg dosis cada 8 horas)
- Tratamiento de los síntomas asociados: vómitos, diarreas, dolor y tratamiento con antibioticoterapia.
- A los pacientes admitidos en la sala de hospitalización se añade oxigenoterapia en caso necesario, garantizando una SO2≥94 %.
Tratamiento específico: Streptococcus pneumoniae es el microorganismo causante de neumonía más habitual en todas las edades pediátricas. El tratamiento antimicrobiano suele ser empírico, ya que no es habitual conocer, con la antelación suficiente, un diagnóstico etiológico que permita establecer un tratamiento basado en él. El tratamiento estándar para las neumonías neumocóccicas es la monoterapia con betalactámicos.(31,32,33,34)
Esquema para uso empírico de antibióticos en niños con neumonías infecciosas bacterianas (la vía de administración dependerá de la gravedad).
- Hasta tres semanas: penicilina G + aminoglucósido (amikacina (15 mg/kg/día) o gentamicina (3-5 mg/kg/día)) c/12 hrs. Neumonías extensas o alérgicos a la penicilina: cefalosporinas de segunda o tercera generación.
- De tres semanas a tres meses: penicilina G cristalina + aminoglucósido (amikacina o gentamicina) o amoxicillina + inhibidores de betalactamasas (sulbactam o ácido clavulánico) o cefalosporina de segunda o tercera generación si hay complicaciones (cefuroxima, ceftriaxona o cefotaxima).
- De cuatro meses a cuatro años: Comenzar con amoxicilina a altas dosis (80-100mg/kg/día) en caso de que tolere la vira oral, de lo contrario se inicia con penicilina cristalina (según el caso, entre 200 000 – 400 000 uds/kg/dosis IM o EV) cada 4-6 hrs (no más de 12 millones por día -2 000 c/4hrs en caso de vía endovenosa, y cada 6 horas por vía intramuscular) según extensión del proceso en pacientes no complicados (24-48 hrs). Si la evolución clínica es favorable, pasar a penicilina procaínica (un millón de uds/m2sc/día) hasta completar diez días de tratamiento. Si la evolución no es buena, reevaluar, sospechar complicación o resistencia bacteriana, y considerar cambio de antibacteriano: Cefalosporinas de segunda generación (cefuroxima 150mg/kg/día en tres subdosis IM o EV-) o de tercera generación (ceftriaxona 100 a 150mg/kg/día en una o dos subdosis, cefotaxima 100-200mg/kg/día en cuatro subdosis).
- Mayores de cinco años: Seguir el mismo esquema antibacteriano del grupo etario anterior y la vía de administración según gravedad del caso. De sospecharse coinfección con mycoplasma o tratarse de una neumonía intersticial, añadir macrólidos (azitromicina 10-15mg/kg/día en una o dos subdosis 5-6 días o claritromicina 14mg/kg/día en dos subdosis 7-10 días).
Criterios de ingreso en UCI
Toda NAC grave debe ser tratada en una UCI pediátrica, por el alto riesgo de complicaciones y mortalidad. Independientemente de la edad, se debe iniciar un tratamiento antibiótico de amplio espectro. Los criterios de ingreso se describen a continuación:
- Signos de insuficiencia respiratoria (Saturación de oxígeno en sangre arterial menor de 92 % con FiO2 > 0,6, distrés respiratorio grave, signos de agotamiento respiratorio, respiración irregular o apneas).
- Presencia de sepsis.
- Grandes opacidades radiológicas.
- Derrame pleural de mediana y gran cuantía.
- Presencia de complicaciones.
- Inestabilidad hemodinámica dada por neumonía:
- Shock séptico.
- Insuficiencia cardiaca congestive.
- Enfermedad coexistente que pueda facilitar una mala evolución.
- Inmunodeficiencias congénitas o adquiridas.
- Daño neurológico severo.
- Cardiopatías congénitas.
- Enfermedad pulmonar crónica reagudizada: displasia broncopulmonar, fibrosis quística.
- Insuficiencia renal.
- Síndromes aspirativos.
Tratamiento de la neumonía grave
Ante la imposibilidad de disponer de un diagnóstico etiológico, el tratamiento antimicrobiano es empírico, con una pauta de tratamiento en función de la edad de los pacientes:
- Recién nacidos hasta tres meses (en caso de neumonía típica o probablemente bactariana): El tratamiento debe iniciarse con ampicilina a 100-200 mg/kg/día (cubre contra listeria y estreptococo beta hemolítico del grupo B) más cefotaxima (100-200 mg/kg/día). Si se sospecha S. aureus, se debe comenzar con vancomicina (60mg/kg/día) asociada a la cefotaxima.
- Pacientes de tres meses de edad en adelante: cefotaxima a 200 mg/kg/día. Si existe empiema, o derrame pleural de mediana o gran cuantía, se adicionará vancomicina a 60 mg/kg/día. Los derrames de pequeña cuantía no requerirán vancomicina.
Se debe adicionar al tratamiento, azitromicina oral 10 mg/kg/día si el patrón radiológico es dudoso de neumonía bacteriana por tener elementos de infiltrado intersticial y por tanto ser probable una neumonía por mycoplasma pneumoniae. Alternativo a este último se pudiera usar levofloxacina IV, 10 mg/kg cada 12 horas (dosis máxima: 750 mg/kg cada 12 horas).
El tratamiento alternativo en caso de alergia a las cefalosporinas, u otra situación, es levofloxacina a la misma dosis expuesta anteriormente. Como tercera variante se usará meropenem IV, a dosis de 100mg/kg/día.
Como tratamiento alternativo a la vancomicina se podrá usar clindamicina IV a dosis de 40 mg/kg/día (cada 8 horas) o linezolid a 30 mg/kg/día (cada 12 horas).
En dependencia de la situación epidemiológica, y según orientaciones administrativas, se usará oseltamivir a 3mg/kg/día cada 12 horas por cinco días, en aquellos pacientes cuyo patrón radiológico ofrezca dudas a favor de una neumonía bacteriana lobar clásica por neumococo.
Criterios de alta hospitalaria
Como criterios de alta hospitalaria se consideran la desaparición de las manifestaciones clínicas, normalización del leucograma y reducción en un 30 % de la cifra inicial en eritrosedimentación y/o proteína C reactiva; así como la mejoría evidente del cuadro radiológico, cuya placa evolutiva no será necesaria en todos los casos, si la evolución clínica y humoral evidencia curación del proceso neumónico.
[1] Leyenda: (++++) más común; (+++) muy común; (++) común; (+) raro; ADV: adenovirus; PI: parainfluenza; VRS: virus sincitial respiratorio.
CONCLUSIONES
En el medio que sirve de contexto a esta Guía, el diagnóstico y tratamiento en la mayoría de los casos de NAC se realiza en el ámbito de atención primaria, con una alta tasa de incidencia. Aunque muy pocos pacientes precisan ingreso hospitalario, el diagnóstico etiológico y la optimización del tratamiento antibiótico continúan siendo un reto difícil de vencer.
Conflicto de interés: Los autores declaran que no existen conflictos de intereses.
Contribución de los autores: idea conceptual: Mercedes Fonseca Hernández, Dáylin Madruga Jiménez; revisión de la literatura: Orlando Morera Álvarez, Elizabeth Ríos Alberdi; escritura del artículo: Dáylin Madruga Jiménez, Orlando Morera Álvarez, Elizabeth Ríos Alberdi; revisión crítica: Mercedes Fonseca Hernández.
Financiación: Hospital Universitario Pediátrico Paquito González Cueto.

