INTRODUCCIÓN
Las cardiopatías congénitas (CC) se presentan aproximadamente en 8 de cada 1000 recién nacidos vivos. La incidencia es mayor en los mortinatos (2 %), los abortos (10-25 %) y los lactantes prematuros (alrededor del 2 %, incluida la comunicación interventricular). Entre los niños con alteraciones cardíacas congénitas existe un espectro amplio de gravedad; aproximadamente 2 o 3 de cada 1000 recién nacidos presenta una CC sintomática en el primer año de vida. El diagnóstico se alcanza durante la primera semana de vida en el 40-50 % de los pacientes y durante el primer mes en el 50-60 %. Cuando se analiza la frecuencia relativa de las CC, exceptuando el conducto arterioso persistente en el neonato pretérmino, la válvula aórtica bicúspide, la estenosis pulmonar periférica y el prolapso de la válvula mitral; la comunicación interventricular (CIV) ocupa el mayor porcentaje de todas las CC con un 25-30 % seguida de la comunicación interauricular (CIA y el conducto arterioso persistente (PCA) ambos con una frecuencia de 6-8 %. Se desconoce la etiología de la mayor parte de las CC. Durante mucho tiempo se ha sabido que los factores genéticos desempeñan un papel importante en la aparición de las cardiopatías congénitas, por ejemplo, algunos tipos de CIV (supracristal) son mas frecuentes en niños de origen asiático. Además el riesgo de recurrencia de una cardiopatía aumenta de 0,8 a 2-6 % cuando un familiar de primer grado (padre o hijo) también está afectado. (1) Se ha considerado a la CIV como un modelo excelente para el estudio de la interrelación anatómica y fisiológica en las diferentes lesiones que permiten una comunicación entre los circuitos pulmonar y sistémico. (1) La CIV consiste en una abertura en el tabique interventricular (TIV) que pone en comunicación a ambos ventrículos y que puede ser de tamaño variable, única o múltiple, aislada o asociada a otros defectos cardíacos. (2,3)
Con esta revisión se pretende: actualizar y profundizar en el conocimiento de una de las cardiopatías de mayor incidencia en la infancia, siendo la más frecuente en el municipio Moa y en Cuba.
DESARROLLO
Historia
En 1879 Roger, es el primero en definir los signos clínicos subyacentes a la CIV, en 1847 Einsenmenger describe los hallazgos post-morten y en 1897 Dalrymple es el primero en acuñar esta entidad con el término de complejo de Einsenmenger. Heath y Edwards en 1958 describen los cambios morfológicos asociados a la enfermedad vascular pulmonar y lo agrupan en 6 categorías comparables con la clasificación actual.
Epidemiología
La CIV constituye aproximadamente el 20 % de las cardiopatías congénitas, si se analiza como lesión aislada. La mayor parte de los centros reportan la CIV como la lesión cardíaca más comúnmente encontrada exceptuando la válvula aórtica bicúspide.
Este tipo de defecto se produce entre el 1,5 – 3,5 por cada mil nacidos vivos y es más frecuente en prematuros, con una incidencia de 4,5 a 7 casos por mil nacidos vivos. Es la cardiopatía congénita que más se asocia a los síndromes cromosómicos incluyendo trisomía 13, 18 y 21, así como síndromes raros asociados con los grupos 4, 5 y C de mosaicismo, además del síndrome de Apert y síndrome de Maullido de Gato, aunque en el 95 % de los casos la CIV no está asociada a anomalía cromosómica. En algunos estudios se informa una frecuencia ligeramente mayor en el sexo femenino (Hoffman y Rudolf, 56 % mujeres y 44 % hombres). (4,5)
Embriología
El tabique interventricular tiene cuatro orígenes embriológicos.
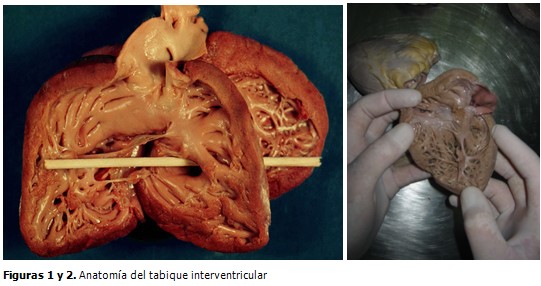
La invaginación muscular, tabique troncoconal, los rebordes endocárdicos. Por último, la conexión de la aorta al ventrículo izquierdo. (6,7) (Figuras 1 y 2).
El tabique interventricular normal por su cara derecha presenta una superficie moderadamente convexa y totalmente trabeculada. Unas de las trabéculas, la septomarginalis, continúa por uno de sus extremos con la cresta supraventricular y por el otro con la banda moderadora, entre estas estructuras quedan delimitadas las porciones de entrada y salida de este ventrículo. El septum interventricular por su superficie izquierda es moderadamente cóncavo y liso en sus dos tercios superiores. Por esta cara no existe ninguna estructura que delimite los tractos de entrada y salida de este ventrículo. (7) La región membranosa del septum interventricular queda situada por detrás de la cresta supraventricular e inmediatamente por debajo de la parte anterior del anillo tricuspídeo y por su cara izquierda se ubica por debajo de los anillos aórtico y mitral, extendiéndose desde la mitad posterior de la sigmoidea aórtica coronariana derecha hasta la parte anterior del anillo mitral. La zona del septum interventricular que queda por detrás del septum membranoso y en relación con los orificios atrioventriculares se denominan septum basal posterior. La zona del septum interventricular que queda por delante de la cresta supraventricular y en relación con las sigmoideas aórtica y pulmonar se denomina septum basal anterior. El resto del tabique interventricular que queda comprendido entre estas tres zonas basales descritas se denomina septum apical o muscular. (8)
Clasificación
Se han hecho numerosas clasificaciones de este tipo de defecto. Una de las más utilizadas sigue siendo la anatómica que hacen Soto y col. que la divide en:
- Perimembranosas:
Única: con extensión muscular, al tracto de entrada y al tracto de salida.
Muscular: trabecular, de tracto de entrada, de tracto de salida.
Subarteriales: sub-aórticas, sub-pulmonar, doblemente relacionada.
Desde el punto de vista clínico se dividen en: ligeras, moderadas o severas, con síndrome de Einsenmenger y la tipo de Small-Horn.
Dicho síndrome lo conforma un tipo de CIV en la que existen dos pequeños cuernos que nacen de la porción alta del septum y que en algunas ocasiones producen obstrucciones en uno o ambos tractos de salida. De acuerdo al estado anatomofisiológico determinado por el tamaño del orificio y la relación entre resistencia vascular pulmonar y sistémica se clasifican en:
- CIV pequeña con disminución de la resistencia pulmonar y/o normal.
- CIV moderada con resistencia pulmonar variable.
- CIV grande con aumento ligero o moderado de la resistencia vascular pulmonar.
- CIV grande con aumento marcado de la resistencia pulmonar (síndrome de Einsenmenger).
Desde el punto de vista ecocardiográfico se clasifica según la relación QP/QS y según la relación CIV/Raíz Ao. Por la relación QP/QS, la CIV se puede dividir en: pequeña, moderada y severa; la primera cuando la relación es menor de 1,5; moderado dentro de 1,5-2 y de gran tamaño si es mayor de 2. Si la relación CIV /raíz Ao es menor de 0,5 se considera un CIV pequeño, si está dentro de 0,5-07 será moderada y mayor de 0,7 se considera severa. (6, 7,9)
Etiología
La etiología se considera multifactorial y se asume que la interacción entre la predisposición hereditaria y las influencias ambientales dan por resultado el defecto. Se consideran importantes los siguientes factores: la diabetes, la fenilcetonuria, el consumo de alcohol, síndrome alcohólico fetal y la predisposición a defectos cardiovasculares en la familia. (3)
Fisiopatología
En los pacientes con defectos del tabique interventricular, la sangre pasa desde el ventrículo izquierdo hacia la arteria pulmonar. Desde el punto de vista técnico transita por el ventrículo derecho, pero como se contrae de manera simultánea, el ventrículo derecho no recibe la sobrecarga de volumen; la arteria pulmonar recibe un volumen incrementado de sangre, del mismo modo que la aurícula y ventrículo izquierdo. Los defectos pequeños no se asocian a incremento de las presiones ventricular derecha y arterial pulmonar mientras que en los grandes defectos el incremento de estas presiones hacen que se igualen a las del ventrículo izquierdo. (10) Los efectos hemodinámicos después del nacimiento dependen de los cambios fisiológicos de la circulación sistémica y pulmonar, así como del diámetro del orificio. La situación del defecto en el tabique interventricular carece de importancia. De su diámetro dependerá el grado de cortocircuito, si este es grande el cortocircuito dependerá de la relación entre la resistencia pulmonar y la sistémica. (1, 9,11) La disminución de la resistencia vascular pulmonar se hace de forma progresiva en la primera semana de vida, a medida que esto ocurre se incrementa el cortocircuito de izquierda a derecha, aumenta por consiguiente el flujo pulmonar, el retorno venoso al atrio y al ventrículo izquierdo. El incremento del retorno venoso eleva la presión telediastólica del ventrículo izquierdo, a tal punto, que esa cámara por un llenado diastólico severo supera el límite de su curva de función, y de este modo aparece la insuficiencia contráctil del ventrículo izquierdo. Las resistencias vasculares pulmonares en las comunicaciones interventriculares amplias no caen a niveles normales. Entre los 3 y 6 meses de edad se observa una disminución alrededor del 3-4U/m2 de superficie corporal. Este comportamiento es distinto en pacientes con corazones normales donde la caída es hasta 2U/m2 de superficie corporal. (12) Se pueden identificar cuatro estados anatomofisiológicos determinados por el tamaño del orificio y el valor de la relación entre la resistencia vascular pulmonar y la resistencia vascular sistémica. (9,13)
CIV pequeña con disminución de la resistencia pulmonar y/o normal
El defecto impone gran resistencia al flujo con gran diferencia de presión en los ventrículos durante la sístole, existiendo un cortocircuito de izquierda a derecha.
(CIV menor o igual de 0,5 cm/m2 de superficie corporal). Las CIV pequeñas están localizadas fundamentalmente en el tabique muscular y no permiten incremento de las resistencias pulmonares. La maduración de las arteriolas pulmonares sigue el curso habitual de un corazón sano. EL grado cortocircuito es variable y dependerá del diámetro del defecto. En estos pacientes la presión sistólica del TAP es normal; estos defectos con frecuencia se cierran en los dos primeros años de vida, en otros casos el cierre espontáneo ocurre más tarde.
CIV moderada con resistencia pulmonar variable
Muchos tienen cortocircuito de izquierda a derecha, de moderada a grande, con sobrecarga de volumen de aurícula y ventrículo izquierdo (por aumento del retorno venoso pulmonar a aurícula izquierda) o hipertrofia ventricular izquierda, siendo inusual un aumento marcado de la resistencia vascular pulmonar. Puede haber pequeños cortocircuito de derecha a izquierda en el período de relajación isovolumétrica.
Hay una diferencia de presión sistólica entre los dos ventrículos durante la eyección ventricular mayor de 15 mmHg. (CIV igual a 1cm/m2 superficie corporal). Las CIV medianas presentan áreas variables. En estas circunstancias la fisiopatología dependerá del área del defecto. Cuando la presión sistólica del ventrículo izquierdo es mayor de un 50 % de la presión sistémica, estos pacientes pueden desarrollar resistencia vascular pulmonar elevada, al igual que los portadores de CIV grandes. Cuando la presión sistólica del ventrículo derecho está entre 40-75 % de la sistémica, aparece la insuficiencia cardíaca.
CIV grande con aumento ligero o moderado de la resistencia vascular pulmonar
A causa del carácter no restrictivo del defecto, la circulación pulmonar está sujeta a la fuerza de eyección de ambos ventrículos durante gran parte de la sístole. En el inicio de la sístole, la presión aumentada del ventrículo izquierdo provoca cortocircuito de izquierda a derecha antes de la apertura de la válvula aórtica. Durante la sístole tardía y el período de relajación isovolumétrica hay cortocircuito de derecha a izquierda, y en la diástole el cortocircuito es bidireccional.
CIV grande con aumento marcado de la resistencia pulmonar. (Síndrome de Einsenmenger)
Si la CIV es amplia existirá hipertensión ventricular derecha similar a la aórtica y a la del ventrículo izquierdo. Habitualmente esto ocurre cuando el diámetro de la comunicación es similar o mayor que la aórtica. Como la resistencia pulmonar cae después del nacimiento, habrá flujo preferencial hacia los pulmones, estableciéndose el cortocircuito de izquierda a derecha. El período de eyección temprano está asociado con cortocircuito de izquierda a derecha (válvula aórtica cerrada), en la sístole media y tardía, así como en la relajación isovolumétrica, cortocircuito de derecha a izquierda. Existe una mejoría del cuadro clínico asociándose además hallazgos similares a los observados en la tetralogía de Fallot, fundamentalmente la cianosis que aparece incluso en reposo y que es más frecuente en el adolescente y en el adulto joven, y es raro en los niños de 2 a 3 años. (9, 13-15)
Cuadro clínico
Los defectos pequeños cursan sin síntomas, aunque pueden instalarse en ellos una endocarditis infecciosa. EL soplo se constata entre las 2 y 6 semanas de vida, aunque pudiera ser antes si el defecto es muy pequeño. En la CIV muscular pequeña el soplo es más rasposo y hay que diferenciarlo con una estenosis pulmonar. Puede estar localizado en cualquier parte del septum interventricular, lo que lo distingue es que siempre tiene una banda muscular.
En la CIV moderada, aparecen síntomas que traducen un aumento del cortocircuito de izquierda a derecha como taquicardia, con esfuerzo inspiratorio aumentado, sudoración excesiva y fatiga a la alimentación. En los pretérmino los síntomas comienzan antes que en los niños normales a término, otro síntoma significativo es la sepsis respiratoria a repetición. (16)
Al examen físico (16-19)
- Inspección: retraso pondoestatural.
- Palpación: precordio activo, frémito con iguales características al anterior.
- Auscultación: 1er ruido aumentado en frecuencia por aumento del volumen diastólico final, 2do ruido desdoblado constante, soplo holosistólico, áspero en borde esternal izquierdo bajo, se puede auscultar en epigastrio (soplo de regurgitación), 3er ruido prominente con retumbo mesodiastólico mitral en ápice (frecuente cuando el flujo pulmonar es dos veces el flujo sistémico y traduce un aumento del flujo a través de la válvula mitral).
En los pacientes con defectos grandes se observa:
a) Niños delgados o desnutridos con taquipnea, sudoración frecuente y retraso en el crecimiento. Exhiben síntomas compatibles con insuficiencia cardiaca crónica con períodos de agudización.
b) Infecciones respiratorias frecuentes.
c) Cianosis
- Persistente desde el nacimiento.
- Durante las primeras semanas de vida, transitoria por el patrón fetal pulmonar.
- Después de la infancia por inversión del shunt, a causa de: enfermedad vascular progresiva estenosis infundibular importante (Fallotización del CIV).
d) Hemoptisis 33 % en edad adulta por hipertensión pulmonar severa.
Al examen físico si existe aumento moderado de la resistencia vascular pulmonar se encuentra: (11, 12,20)
- Inspección: precordio hiperactivo, aumento del diámetro anteroposterior del tórax.
- Palpación: galope del ventrículo izquierdo en ápice, frémito, actividad difusamente aumentada en precordio, impulso sistólico del TAP y P2 palpable.
- Auscultación: 1er ruido normal o disminuido, 2do ruido con desdoblamiento estrecho, soplo localizado en área del ventrículo derecho decreciendo y que desaparece en la telesístole (disminuye de intensidad y se hace más corto). 3er ruido con retumbo mesodiastólico en ápice (signos de repercusión hemodinámica), soplo sistólico eyectivo en borde esternal izquierdo alto (chasquido protosistólico), solplo diastólico débil en foco pulmonar (escape pulmonar).
En los pacientes con defectos grandes y un aumento marcado de la resistencia vascular pulmonar al examen físico:
- Inspección: no hay corazón hiperdinámico.
- Palpación: ventrículo derecho e impulso el TAP palpables, P2 palpable.
- Auscultación: 2do ruido usualmente único o poco desdoblado, soplo holosistólico que desaparece en la telesístole, a veces es muy corto o desaparece, no hay retumbo, 3er ruido en borde esternal derecho.
Cuando hay cambios en las características del soplo, este disminuye de intensidad con desaparición del frémito sistólico hay que pensar en:
- Que el agujero se esté cerrando (45-80 % en los primeros 3 años de vida hasta los 9 años).
- Que esté evolucionado a una hipertensión pulmonar.
- Que se esté produciendo una obstrucción del tracto de salida del ventrículo derecho (del infundíbulo), o sea Fallotización del CIV. Hacen crisis de hipoxia y se diferencia por las características del 2do ruido.
- Que la valva septal de la tricúspide parchee el defecto.
En resumen existen diferentes caminos en la evolución natural de la CIV, dentro de estos se pueden mencionar: cierre espontáneo del defecto (30-40 %), insuficiencia cardíaca, infecciones respiratorias a repetición, desnutrición, parche septal tricuspídeo, parche septal aórtico, endocarditis infecciosa, Fallotización del CIV, hipertensión pulmonar, síndrome de Einsenmenyer, muerte. (1, 4, 20,21)
Causas de cierre completo o incompleto de la CIV
La CIV puede tener un cierre espontáneo sin necesidad de un parche quirúrgico. Entre estas modalidades se encuentran: fusión de la valva septal de la tricúspide con la CIV, hipertrofia del tabique interventricular por proliferación del tejido fibroso, prolapso de la válvula aórtica, endocarditis infecciosa, aneurisma del septum interventricular (lo que ocasiona arritmias, obstrucciones al tracto de salida del VD, ruptura y comunicación ventrículo atrial).
Anomalías asociadas
Coartación aórtica, estenosis pulmonar, atresia tricuspidea, doble emergencia del VD, transposición de grandes vasos, tetralogía de Fallot, síndrome de hipoplasia de cavidades izquierdas, atresia pulmonar.
Complementarios
Radiología: en los defectos pequeños, el corazón es de tamaño normal al igual que le flujo pulmonar. Cuando el CIV es moderado la cardiomegalia es variable y existe un hiperflujo pulmonar con elongación y posición lateral del ápice. En los defectos grandes con resistencia vascular pulmonar moderadamente aumentada existe cardiomegalia generalizada con flujo pulmonar aumentado, un TAP prominente y el diafragma en posición baja. En los casos de resistencia vascular pulmonar (RVP) severamente aumentada, el corazón es de tamaño normal con hipertrofia de ventrículo derecho y ápice levantado, prominencia del TAP y el flujo pulmonar aumentado en el tercio externo de ambos campos pulmonares. (1, 11,22)
Electrocardiograma: el electrocardiograma de los pacientes con CIV pequeño es completamente normal. En los defectos más grandes se encuentran signos de sobrecarga diastólica de ventrículo izquierdo (R altas en derivaciones izquierdas, T positiva alta con supradesnivel del ST y Q estrecha y profunda en V5 y V6). Existe en estos defectos también una onda P bimodal y un eje eléctrico desviado hacia arriba y la izquierda. Cuando existe hipertensión pulmonar el eje está en el plano frontal con signos de sobrecarga sistólica de ventrículo derecho y onda P pulmonar. (8, 15,23)
Ecocardiograma: la ecocardiografía es importante para precisar la localización y el diámetro del defecto (se visualizan defectos septales > de 3 mm), permite constatar la dilatación de cavidades izquierdas por cortocircuito de izquierda a derecha y para evaluar el estado contráctil tanto de ventrículo izquierdo como del ventrículo derecho. Además permite el diagnóstico de anomalías asociadas, el cálculo de la relación CIV / raíz aorta y QP/QS, esta última con el uso del Doppler. Con la ecocardiografía Doppler se puede verificar la turbulencia sistólica que lo distingue del flujo aurículo ventricular que es diastólico, y con el color se verifican los cortocircuitos de izquierda a derecha y de derecha a izquierda, así como la localización del defecto según la clasificación anatómica. Es de gran importancia la medición de las presiones pulmonares y el hallazgo en caso de hipertensión pulmonar de signos de hipertrofia ventricular derecha así como insuficiencia tricuspídea (9, 18,24)
Cateterismo
Indicaciones:
Todo niño con insuficiencia cardíaca o con evidencia de gran CC-ID sin insuficiencia cardíaca, pacientes con CC-ID moderado o grande donde se contempla la cirugía.
Cineangiografía:
Es obligatorio en todo paciente que se le va a realizar tratamiento quirúrgico para conocer:
Localización y número de defectos, distribución de las arterias coronarias, insuficiencia aórtica. Por aortografía. (Cuando en una CIV hay signos de insuficiencia aórtica la conducta siempre es quirúrgica).
En el desarrollo de la enfermedad pulmonar intervienen varios factores: presencia de una CIV grande, presión de un VI que se transmite prácticamente por igual tanto al circuito aórtico como al pulmonar, hipoxia. (25)
Diagnóstico diferencial
Defectos de cojinetes endocárdicos, tetralogía de Fallot, doble emergencia de VD, estenosis infundibular pulmonar, estenosis subaortica ligera-moderada, tronco arterioso.
Tratamiento
I – Preventivo:
Tiene gran importancia orientar el diagnóstico prenatal a los grupos considerados de riesgo, lo que debe jerarquizarse por la consulta de genética. Forma parte también de la prevención (secundaria) el evitar la endocarditis infecciosa cumpliéndose con los esquemas establecidos para ella.
II – Médico:
El tratamiento en los pacientes con CIV pequeñas solo consiste en la profilaxis de la endocarditis infecciosa. Cuando existen síntomas de insuficiencia cardíaca entonces hay que incorporar al tratamiento drogas como los digitálicos, los diuréticos, vasodilatadores y suplementos de potasio. Es de vital importancia el apoyo nutricional del paciente así como el apoyo psicológico al familiar. (16, 18,26)
III – Quirúrgico:
En el tratamiento quirúrgico por circulación extracorpórea convencional el CIV se puede hacer a través de la aurícula derecha, del VD, de las grandes arterias, y de la punta del VI. La vía de abordaje depende de la localización del CIV. En la CIV perimembranosa se puede realizar una atriotomía derecha y cierre a través de la válvula tricúspide con goretex, dacrón o parche pericardio. Dentro de las secuelas se encuentran: la insuficiencia pulmonar, bloqueo AV y derrames, y entre los residuos más frecuentes: las dehiscencias del parche, el shunt residual, la estenosis infundibular y la insuficiencia aórtica ligera.
Existen una serie de criterios quirúrgicos establecidos a partir de la evaluación de parámetros clínicos, ecocardiográficos y de cateterismo que se resumen en los siguientes:
- Insuficiencia cardíaca irreductible, bronconeumonía a repetición, retardo pondoestatural marcado. En mayores de 3 meses con los criterios anteriores o QP/QS >= 2, CIV/Ao > 0,75. En menores de 3 meses con criterios clínicos anteriores y CIV múltiple: cerclaje pulmonar, en mayores de un año de edad: cateterismo. Si CC-DI.
La mortalidad quirúrgica se encuentra entre 2-5 % (19, 26,27)
En la actualidad, las técnicas de cierre por medio de catéter han sido aplicadas a las formas congénitas y adquiridas de los defectos del TIV con objeto de eliminar la necesidad de reparación quirúrgica o reducir el riesgo o complejidad de esta. (25) Se han empleado el dispositivo Clamsgell, (26) el de doble sombrilla de Rashkind (CRBARD) (27) y los dispositivos en botón (Custom Medical Devices), (27) para cerrar los defectos de las porciones musculares y perimembranosas del TIV con buenos resultados, así como el amplatzer.
Rehabilitación
A partir de la formación en 1963 del Comité de Expertos de la Organización Mundial de la Salud (OMS) en enfermedades cardiovasculares, han ocurrido importantes cambios en los métodos de rehabilitación de este tipo de pacientes, desde esa fecha pediatras y cardiólogos comenzaron a estudiar profundamente el ejercicio físico como una forma de mejorar la calidad de vida de estos niños. En la actualidad la rehabilitación está considerada como una parte esencial de la atención y la terapéutica, a la que debe tener acceso todo paciente cardiópata de cualquier edad para mejorar su calidad de vida. (27)
CONCLUSIONES
La CIV continúa siendo una cardiopatía congénita de incidencia significativa. Entre varias clasificaciones, la anatómica de Soto es la más utilizada. El defecto septal y la resistencia vascular pulmonar determinan la hemodinamia de la CIV. La evolución natural tiene diferentes caminos, determinando el pronóstico y la terapéutica a emplear. En la actualidad, las técnicas de cateterismo terapéutico han reemplazado a las operaciones ordinarias de muchas lesiones. En la actualidad la rehabilitación está considerada como una parte esencial de la atención y la terapéutica, a la que debe tener acceso todo paciente cardiópata de cualquier edad para mejorar su calidad de vida.
Es de vital importancia actualizar y profundizar en el conocimiento de la CIV, por ser una de las cardiopatías de mayor incidencia en la infancia, tanto en el municipio en el que se realizó el estudio como en todo el país. Por lo que los especialistas implicados en realizar su diagnóstico y tratamiento oportuno, deben contar con las herramientas necesarias para llevar a cabo esta labor.