INTRODUCCIÓN
El sueño es un estado fisiológico y conductual, reversible, recurrente, metabólicamente activo, donde se manifiesta actividad eléctrica cerebral y se produce reorganización del sistema nervioso con desaferentación externa y modificación de las conexiones neuronales.
Es un proceso activo que al igual que el estado de la vigilia, está regido por mecanismos neurofisiológicos, neuroendocrinos e inmunológicos que permiten un desarrollo favorable de las funciones físicas y psíquicas del organismo durante las diferentes etapas del desarrollo del ser humano, principalmente en la infancia y adolescencia. (1,2)
Los trastornos del sueño (TS) son un problema prevalente en la atención primaria pediátrica, que afecta aproximadamente a un 30 % de la población infantil, estos trastornos están agrupados según la International Classification of Sleep Disorders (ICSD) en cuatro categorías: (3,4)
- Disomnias: dificultad para iniciar o mantener el sueño (insomnio) o dificultades por exceso de sueño (hipersomnia).
- Parasomnias: trastornos del sueño que no causan primariamente insomnio ni hipersomnia. Son expresiones de la activación de sistemas fisiológicos en momentos inapropiados del ciclo sueño-vigilia.
- Alteraciones del sueño asociadas a enfermedades médicas o psiquiátricas.
- Trastornos del sueño no catalogados: alteraciones del sueño de las que no existe información suficiente para considerarlas individualmente como un síndrome (ejemplo: hiperhidrosis nocturna).
En los últimos años, se ha puesto de manifiesto la importancia de la detección y el tratamiento precoz de los TS en el niño, al demostrarse que la alteración de la cantidad y calidad del sueño puede tener repercusiones físicas y cognitivas negativas. Así, los trastornos del sueño, principalmente los secundarios a patologías obstructivas de las vías aéreas superiores, se han visto implicados como posibles causas de retraso del crecimiento, desnutrición proteico-energética, disfunción ventricular, alteraciones de rendimiento académico y problemas conductuales. (5-7)
No existe una definición formalmente aceptada de los Trastornos Respiratorios Asociados al Sueño (TRAS) en niños, los cuales figuran como trastornos intrínsecos del sueño que incluyen según la ICSD en la categoría de las disomnias, caracterizados por una resistencia incrementada u obstrucción parcial prolongada y/o completa de la vía aérea superior que altera la ventilación, la oxigenación pulmonar y la calidad del sueño. (3,8)
Esta definición incluye un amplio espectro de patologías dependientes del grado de resistencia y colapsabilidad de las vías aéreas superiores (VAS) durante el sueño: (3)
- Roncador primario: hay un aumento discreto de la resistencia de las VAS sin apneas asociadas, anomalías en el intercambio de los gases, despertares ni fragmentación del sueño (se conserva el ritmo nictameral). No se conoce su significado clínico. Hay autores que lo asocian con anomalías en el registro eléctrico de la actividad cerebral (EEG) en las fases de sueño profundo y alteraciones en el aprendizaje y/o comportamiento.
- Síndrome de aumento de resistencia de las VAS (SARVAS): estos niños roncan y tienen episodios de obstrucción parcial de la VAS que causan un aumento del esfuerzo respiratorio con arousal y fragmentación del sueño. No hay apneas, hipopneas ni anormalidades en el intercambio de gases.
- Síndrome de apnea-hipopnea del sueño sin desaturaciones: presentan apneas e hipopneas con alteraciones en el ritmo nictameral pero sin desaturaciones de O2.
- Síndrome de apnea obstructiva del sueño con desaturaciones (SAOS): presentan apneas e hipopneas, alteración en la arquitectura fisiológica del sueño y anormalidades en el intercambio de gases (desaturaciones de O2).
El Síndrome de Apnea Obstructiva del Sueño (SAOS) se considera la forma más severa de expresión de los TRAS, al definirse según el Dr. Jordi Coromina otorrinolaringólogo del Centro Médico Teknon de España, como episodios recurrentes de obstrucción parcial y prolongada u obstrucción total e intermitente de las vías respiratorias superiores durante el sueño con persistencia de la actividad de los músculos respiratorios, un reducido o ausente flujo aéreo naso-bucal, hipercapnia y desaturación oxihemoglobínica. (5)
El diagnóstico precoz y tratamiento adecuado de los TRAS en el niño constituyen en estos momentos un reto por considerarse un problema de salud de alta prevalencia, que cruza la frontera de múltiples especialistas (pediatras, neurólogos, neumólogos, otorrinolaringólogos, psiquiatras, odontoestomatólogos...). La evolución clínica y progresión de estos trastornos no solo reduce la calidad del sueño y altera el comportamiento diurno del niño, sino que implica de forma sistémica al organismo, al desencadenar complicaciones que pueden comprometer la vida del paciente. (5, 9,10)
Según Singer y Saenger las manifestaciones pueden ser tan leves como el roncar, tan sutiles como los trastornos del comportamiento, tan graves como la falta de crecimiento, tan amenazantes como el desarrollo de cor-pulmonar y tan dramáticas como la muerte súbita. (11)
Se ha podido constatar un comportamiento de los TRAS en la población infantil de Moa, similar a los referidos por la mayoría de los autores. Sin embargo, nos hemos percatado que en la atención médica que reciben solo se tiene en cuenta la repercusión sobre determinados órganos dianas y no de forma integral como una entidad clínica única.
Por consiguiente, esta revisión bibliográfica pretende como objetivo: difundir los diversos aspectos fisiopatológicos, clínicos y diagnósticos de los TRAS en la edad pediátrica, para contribuir a que se logre un manejo integral precoz al evitar las importantes secuelas del SAOS infantil, como máxima expresión clínica de los trastornos respiratorios asociados al sueño.
DESARROLLO
Epidemiología
Los TRAS en la edad pediátrica y en particular el SAOS se observan por igual en niños y niñas de todas las edades, son más frecuentes entre los 2 y 8 años de edad y especialmente entre los 3 y 6 años, debido a que en este periodo de edad, la relación entre las estructuras anatómicas de la vía aérea superior y el tejido linfoide local hacen que el calibre de la vía aérea sea menor. (4, 5,7)
Los reportes de prevalencia del ronquido primario en el niño varían entre el 3,2 y el 34,5 % según encuestas creadas y validadas para estudiar los TRAS en la infancia. El comportamiento epidemiológico del SAOS ha sido muy difícil de precisar debido a que no existen estudios amplios de prevalencia. Los reportes más difundidos utilizan la polisomnografía (PSG) como método diagnóstico, sin embargo constan de pocos casos y siempre se realizan en poblaciones seleccionadas. Las series más numerosas se basan en la baremación de cuestionarios clínicos de difícil aceptación por su baja especificidad y sensibilidad. Dependen de la procedencia, los criterios diagnósticos, (PSG o características clínicas), el rango de edad de la muestra y de los puntos de corte del índice Apnea-Hipopnea (IAH), la cifra varía entre el 1-3 %. (5, 12,13)
Etiología
La causa más frecuente del SAOS en el niño es la hipertrofia adenoamigdalar aunque se ha comprobado que la gravedad de esta, no siempre tiene correlación con la dimensión de las amígdalas o de las adenoides. Coromina plantea que: ¨la hipertrofia adenoamigdalar no interviene como única causa de las alteraciones respiratorias observadas durante el sueño, sino que precipitaría el SAOS en aquellos niños con previas alteraciones funcionales de las vías aéreas superiores¨. (2, 4, 5,13)
Se han descrito otras causas importantes de TRAS y SAOS en la infancia las cuales se agrupan según el mecanismo patogénico en: trastornos anatómicos, alteraciones neuromusculares y misceláneas. (Tabla 1).
Fisiopatología
La fisiopatología del SAOS y sus implicaciones clínicas son complejas, multifactoriales y no entendidas completamente, sin embargo la mayoría de los autores coinciden en que se debe a una obstrucción de las VAS durante la inspiración, fenómeno que alcanza su máxima expresión en la fase de Movimientos Oculares Rápidos (MOR) del sueño. (4,5)
En condiciones normales existe un equilibrio entre las fuerzas que tienden a cerrar o colapsar las VAS (presión inspiratoria intraluminal negativa) y las presiones que tienden a abrirlas (músculos dilatadores de la faringe) al garantizar de esta forma una adecuada ventilación pulmonar.
Los factores predisponentes o causales del SAOS, aumentan la resistencia de las VAS (alteraciones anatómicas) y/o disminuyen la actividad de los músculos dilatadores de la faringe (alteraciones neuromusculares) que provocan que la balanza se desequilibre, aumente la presión crítica (presión exterior de la zona colapsable de la faringe) y desencadenen diferentes grados de obstrucción. (9, 14,15)
Por otro lado el sueño es considerado el factor funcional más evidente que predispone al SAOS. Durante la fase MOR se produce una reducción tan marcada de la actividad de los músculos que mantienen la vía aérea permeable, que el SAOS pediátrico podría considerarse una enfermedad de esta fase del sueño. (5)
La repercusión clínica del SAOS infantil depende de las características anatómicas y funcionales de la faringe del niño y de la frecuencia e intensidad de obstrucción que sufra la VAS. Los niños con SAOS presentan de manera predominante hipopneas y con menor frecuencia apneas, es decir, que la obstrucción infantil suele ser parcial y rara vez total. Ello se debe a que el espacio existente entre el paladar blando y la pared posterior de la nasofaringe en el niño, puede expandirse mucho más que en el adulto, ante una obstrucción. Además, el umbral de despertar es mayor, a menor edad del paciente. (5,15)
De un modo constante, se repite siempre la misma secuencia: sueño, hipopnea/apnea, hipoventilación, cambios gasométricos (hipoxemia e hipercapnia) y despertar transitorio que pone fin a la apnea, y coincide con un ronquido intenso o un jadeo, producido por la vibración de los tejidos blandos de la orofaringe (paladar y úvula) al aumentar la velocidad del paso del aire inspirado. Dichos tejidos flamean como una bandera al viento. (4, 5,14)
El despertar transitorio – arousal - o – microdespertar- se produce cuando el esfuerzo inspiratorio alcanza un determinado umbral, en el que los músculos de la vía respiratoria se reactivan, al abrir la faringe. Entonces, la ventilación se reanuda, se corrigen la hipoxia y la hipercapnia, el individuo se vuelve a dormir y el ciclo comienza otra vez. Hay que tener en cuenta que de tal despertar el individuo no es consciente, a pesar del incremento de la actividad electroencefalográfica. (4,5)
Los arousals son respuestas necesarias para sobrevivir, sin embargo, la repetición de estos traducen el grado de severidad de los episodios de apnea o hipopnea que sufre el paciente durante el sueño, los cuales pueden desencadenar reflejos en el centro vasomotor y provocan arritmias (especialmente bradicardia), que son exacerbadas por la isquemia miocárdica secundaria a la hipoxia. (4)
Como consecuencia de la obstrucción de la vía aérea superior, se generan presiones intrapleurales cada vez más negativas al aumentar la postcarga cardíaca. La hipoxemia e hipercapnia mantenidas producen vasoconstricción pulmonar y sistémica, causas potenciales de hipertensión arterial y pulmonar. La suma de estos dos fenómenos son factores determinantes en a aparición del cor-pulmonar. (5,7)
Durante los episodios obstructivos se produce aumento de la actividad del sistema nervioso simpático,
- arousal - (EEG y/o subcorticales), fragmentación del sueño y/o desaturación de la oxihemoglobina. Estos cambios evolucionados en el tiempo pueden conducir a alteraciones del crecimiento, neurocognitivas, psíquicas y cardiovasculares. Así mismo, los episodios de hipoxemia nocturna intermitente se han visto asociados en adultos a una respuesta inflamatoria sistémica con incrementos de la proteína C-reactiva (PCR) y varias citoquinas inflamatorias (interleukinas 6 y 8, factor de necrosis tumoral, moléculas de adhesión intercelular…), y una disminución del óxido nítrico exhalado a nivel alveolar. Estos hallazgos podrían relacionar el SAOS con la aparición del síndrome metabólico. (14)
Manifestaciones clínicas
Las manifestaciones clínicas de los TRAS varían desde el ronquido simple hasta las formas clínicas más graves de SAOS por lo que se considera este como el síntoma guía, su ausencia por lo general descarta el resto de las entidades incluidas dentro de este grupo de patologías. (5,9)
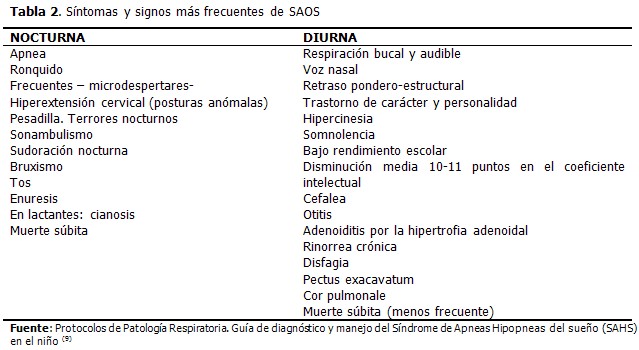
El espectro de manifestaciones clínicas del SAOS en la infancia es muy amplio por lo que tiende a ser dividido en síntomas nocturnos y diurnos para su mejor comprensión e interpretación. (5, 9,13) (Tabla 2).
Los niños con TRAS no manifiestan por lo común despertares clínicamente evidentes durante el sueño, generalmente experimentan microdespertares asociados a respiración ruidosa con hundimiento del tórax, movimientos corporales persistentes o recurrentes, excitación y sudoración por lo que el sueño se hace intranquilo ¨la cama revuelta¨. También son frecuentes los cambios súbitos de posición (de rodillas, sentado o posición genupectoral), a menudo con hiperextensión del cuello, actitudes adoptadas para mejorar la permeabilidad de las vías aéreas superiores durante el sueño. (5)
La somnolencia diurna no es común en niños, a diferencia del adulto, aunque en casos severos estará presente. Su incidencia es la misma que en niños que no roncan. (5)
La mayoría de los infantes con SAOS no son obesos, pero la obesidad los predispone a sufrir SAOS. Aunque lógicamente se recomienda la reducción de peso en todos los niños obesos con SAOS, rara vez tiene éxito y solo retrasa una cirugía (adenoidectomía y reducción amigdalar) inevitable. La causa principal de que la obesidad predisponga al SAOS es la disminución de la luz faríngea, como resultado del depósito de tejido graso en el tejido faríngeo (úvula, paladar, amígdalas, lengua, paredes laterales de la faringe). Ello se aprecia fácilmente mediante resonancia magnética. (5)
Según Chervin y Guilleminault, los niños que roncan (roncadores simples), tienen un riesgo dos veces superior de padecer un síndrome de hiperactividad y déficit de atención. Este riesgo se eleva al triple en los niños menores de ocho años que sufren SAOS. (16)
Otras alteraciones frecuentes son la conducta agresiva y rebelde, la timidez patológica, y el fracaso escolar. Para David Gozal, el SAOS infantil no tratado, provoca una pérdida media en el coeficiente de inteligencia de 10-11 puntos. También insiste en que el SAOS causa estragos cuando el niño ingresa en el sistema escolar y se le fuerza a sentarse en clase y a escuchar al profesor. (9, 17,18)
Es entonces cuando, según nuestras experiencias, se detecta generalmente la hiperactividad y por ello son remitidos a la consulta de psiquiatría infantil sin comprobar previamente si roncan o tiene problemas respiratorios durante el sueño.
El retraso del crecimiento es uno de los principales rasgos del SAOS avanzado en la infancia. Se plantea que el fallo de medro es secundario a la anorexia, la disfagia, la disminución de la síntesis de la hormona del crecimiento y de los factores de crecimiento semejante a la insulina IGF-1 e IGF BP-3, (pico máximo de producción durante el sueño nocturno) y al aumento del gasto calórico, debido al incremento del esfuerzo respiratorio y la sudoración nocturna. (5,9)
En un estudio inicial que se realizó para definir si el cuestionario TuCASA (14) era fiable para ser aplicado en la población infantil cubana, se pudo constatar que la mayoría de los niños roncadores habituales encuestados eran delgados a pesar de existir una tendencia al sobrepeso y la obesidad en los escolares de Moa. (19)
Alteraciones del habla:
a) Hiponasalidad o rinolalia closa: fenómeno caracterizado por la nasalización de la voz producida por la disminución del flujo de aire a través de las fosas nasales, determinado por la hipertrofia adenoidal.
b) Hipernasalidad o rinolalia abierta: se produce por un mecanismo fisiopatológico exactamente opuesto al anterior: la válvula velofaríngea (velo del paladar y paredes faríngeas) no cierra bien y permite la fuga de aire hacia las fosas nasales al pronunciar locales o consonantes de alta presión. La hiperplasia de las amígdalas constituye la causa más frecuente de rinolalia abierta, ya que al protruir hacia arriba, impiden el cierre completo del paladar blando. (5)
Alteraciones en el desarrollo maxilofacial y de la oclusión
En general, la hiperplasia adenoidal y/o amigdalar producirá la facies adenoidea o cara de cansancio, que incluye: cara larga y estrecha, nariz pequeña y respingona, por ausencia de función del tercio medio facial, boca abierta, retrognatia, maloclusión dentaria, incisivos superiores a la vista, labio superior corto, labio inferior grueso y evertido, hipoplasia de senos maxilares, del maxilar superior y de la mandíbula. (2,5)
Enuresis nocturna
El SAOS infantil es una causa reconocida de enuresis nocturna. En muchas ocasiones la corrección del SAOS ocasiona la desaparición de la enuresis. La incidencia de enuresis en niños roncadores de 4 o más años, es de un 41 %, frente al 5 - 15 % de la población general. Basha estudió 57 niños mayores de 4 años con SAOS y enuresis nocturna.
Tras el tratamiento quirúrgico (adenoidectomía y cirugía amigdalar) se produjo la desaparición de la enuresis en un 61 % de casos y una reducción significativa en el 23 %. (18)
Diagnóstico
El diagnóstico de SAOS infantil puede realizarse mediante la historia clínica, el examen físico, el registro de video o audio del sueño del niño, la pulsometría/capnografía nocturna y el estudio polisomnográfico. El estudio polisomnográfico es en la actualidad la mejor metodología para confirmar el diagnóstico y evaluar la gravedad del SAOS.
Algunos autores consideran que una buena aproximación al diagnóstico inicial del SAOS infantil, podría realizarse mediante la clínica, un video doméstico y la poligrafía cardiorrespiratoria. Sin embargo, esta última solo analiza las variables cardiorrespiratoria (flujo nasal, el movimiento torácico, la posición corporal y la frecuencia respiratoria y cardíaca) y excluye las variables neurofisiológicas. (5, 6,20)
Historia clínica y examen físico
Es muy improbable que los niños puedan presentar SAOS sin ronquido. Por lo tanto, debería ser de rutina el investigar este síntoma. Asimismo, es importante preguntar a los padres si han observado apneas o paradas respiratorias durante el sueño de sus hijos, sueño agitado, enuresis, cianosis, excesiva somnolencia diurna, alteraciones del comportamiento o dificultades en el aprendizaje. (1,2)
En el año 2002 la Academia Americana de Pediatría dicto un grupo de recomendaciones para el diagnóstico del SAOS en niños las cuales se mantienen vigentes. (20) (Tabla 3).
El diagnóstico anatómico o de localización de la causa obstructiva, es muy importante en la población infantil, dado que en el niño estos factores tienen más protagonismo. Por ello es especial una exploración básica del área otorrinolaringológica (ORL) y maxilofacial.
Examen físico
El examen físico puede ser normal, pueden hallarse anormalidades no específicas o bien podrían estar presentes algunas de las complicaciones del SAOS. En primer lugar, se inspeccionará el aspecto externo del niño, quien suele ser un respirador oral crítico, con facies adenoidea característica y retrognatia, raramente hay prognatismo. No es frecuente hallar la obesidad tan típica en los adultos y sí en cambio un retraso en el desarrollo ponderoestatural, que en muchos casos se ha demostrado reversible con la resolución del SAOS. (5,6)
En segundo lugar, se explorará meticulosamente la cavidad oral: tamaño de las amígdalas, forma del paladar duro y blando, el frenillo lingual (anquiloglosia). Será importante ver si el cierre y oclusión de la arcada dentaria es correcto. Si el niño colabora, se debe realizar una fibroendoscopia (de nariz, cavum y laringe), al descartar si hay o no hipertrofia adenoidal, desviación del tabique nasal, hipertrofia de cornete, pólipos nasales y/o de rinofaringe. También se visualizará la cara nasal del paladar blando, su funcionamiento y si su cierre está impedido por la obstrucción del polo amigdalar superior. En caso de no contar con esta tecnología se realizará la exploración del adenoides a través del tacto nasal posterior. (5)
Estudios imagenológicos
Radiografía simple lateral de las partes blandas de cráneo o cavum: normalmente el crecimiento del adenoides está sincronizado con el descenso del maxilar superior, que al alejarse de la base del cráneo condiciona un aumento del tamaño de la rinofaringe. Cuando este equilibrio se pierde y las vegetaciones crecen más de lo debido o el cavum es hipoplásico, aparece la obstrucción retronasal. La relación entre ambos volúmenes (adenoides y cavum), es un buen índice para evaluar el grado de obstrucción rinofaríngea causada por la hipertrofia adenoidal.
La cefalometría (radiografía cefalométrica lateral), permiten una valoración objetiva del esqueleto facial. Son baratas, fácilmente accesibles y útiles para valorar y medir: la retrognatia, el espacio posterior de la vía respiratoria o distancia desde la lengua a la pared faríngea posterior y el grosor del paladar blando, que suele ser mayor en individuos con SAOS. Su principal inconveniente es que dan una imagen bidimensional de estructuras que en realidad son tridimensionales.
Otras técnicas radiológicas son: la resonancia magnética nuclear, que proporciona una reconstrucción tridimensional de los tejidos blandos, como la lengua, el paladar blando y la grasa circundante; tomografía axial computarizada ultrarrápida (Cine-Tc), reproduce con precisión las vías respiratorias durante la respiración y los periodos de apnea, además ofrece una reconstrucción tridimensional de las estructuras óseas. El alto coste de estas pruebas, así como la necesidad de sedar o anestesiar al niño, han evitado que se generalice su utilización. (5,6)
La polisomnografía nocturna (PSG) es la única técnica diagnóstica que evalúa cuantitativamente las alteraciones ventilatorias y estructurales del sueño que se manifiestan mientras el individuo duerme, y permiten realizar el diagnóstico diferencial del ronquido primario. (2, 4, 9,12)
Durante la PSG se registran diversas señales electrofisiológicas, como son el electroencefalograma (que detecta fácilmente los microdespertares y permite diferenciar las fases MOR de las no MOR del sueño) y el electromiograma para registrar los movimientos de la pared torácica, el flujo aéreo naso-bucal, la oxigenación (con la pulsioximetría o mediante la monitorización de la presión transcutánea de O2) y las medidas de retención de CO2 (con termistores oronasales y/o sensores de CO2 nasales). Al mismo tiempo, se realiza una monitorización audiovisual del sueño. (5,12)
En el niño, la apnea obstructiva se define como la ausencia de flujo respiratorio naso-bucal en presencia de esfuerzo respiratorio continuo, que se acompaña de una reducción de la saturación de O2 del 4 % y que presenta una duración superior a 2 ciclos respiratorios. La hipopnea obstructiva se define como una reducción del 50 % de la amplitud del flujo naso-bucal en presencia de esfuerzo respiratorio de duración superior a 2 ciclos respiratorios y desaturación de O2 del 4 %. (5, 6,9)
El índice de apnea (IA) o de apnea/hipopnea (IAH) patológicos constituyen pilares en el diagnóstico de SAOS en los niños. El índice de apnea (IA) (o número de apneas por hora) se considera patológico cuando supera 1 evento por hora de sueño (IA > 1/h); el índice de apnea/ hipopnea (IAH) (es decir el número total de apneas e hipopneas por hora de sueño) es patológico cuando supera los 3 eventos por hora de sueño (IAH > 3/h). (5, 9,12)
La polisomnografía nocturna sigue siendo el mejor método diagnóstico, aunque los problemas derivados de su alto coste y de la necesidad de personal adiestrado, siguen provocando el intento de ofertar métodos alternativos. Los estudios polisomnográficos diurnos, más fáciles en niños, tienen el inconveniente de precisar sedación o privación del sueño (lo primero aumenta la obstrucción de la vía aérea superior en sanos, y lo segundo, el número de apneas). Además, la sensibilidad no llega al 80 %, por lo que un test negativo no descarta el diagnóstico, y obliga a la realizar una polisomnografía nocturna. (5)
A pesar de no contar con el equipamiento necesario para lograr evaluar la severidad de la obstrucción de las VAS durante el sueño en los niños roncadores habituales, se puede afirmar, que al realizar un interrogatorio minucioso y de un examen físico exhaustivo, se puede lograr un acercamiento al diagnóstico que permita garantizar un seguimiento y manejo integral adecuado.
Tratamiento
El tratamiento va encaminado a eliminar los factores predisponentes orgánicos o funcionales involucrados en la aparición del SAOS pediátrico. Existen evidencias clínicas y diagnósticas de la relación que guarda la hipertrofia adenoamigdalar con las manifestaciones obstructivas de las vías respiratorias altas durante el sueño, lo cual es considerado en la actualidad el principal criterio de amigdalectomia y adenoidectomia. (5, 6, 9, 20, 21-23)
Coromina en su libro: ¨El niño roncador. El niño con Síndrome de Apnea Obstructiva del Sueño ¨, publicado en el año 2006, da a conocer la técnica y las espectaculares ventajas de la reducción amigdalar con láser, frente a las técnicas tradicionales o clásicas de amigdalectomía total, como tratamiento a los pacientes con SAOS infantil secundario a la hiperplasia adenoamigdalar. Los resultados obtenidos en este estudio, demostraron la desaparición de la sintomatología en el 97 % de los pacientes y la resolución de las alteraciones polisomnográficas entre el 75 % y el 100 % de los casos. (5)
CONCLUSIONES
El SAOS es considerado la forma clínica más grave de los TRAS en la edad pediátrica, al producir una morbilidad significativa entre los 3-6 años de edad, al constituirse la hiperplasia de las amígdalas palatinas y adenoides el principal factor desencadenante. El ronquido nocturno constituye el síntoma guía que orienta hacia el posible diagnóstico de esta entidad, la cual repercute de forma sistémica en el organismo desencadenando complicaciones físicas, cognitivas y neurofisiológicas a corto y largo plazo.
La polisomnografía nocturna constituye el método diagnóstico de mayor especificidad al permitir evaluar cuantitativamente las alteraciones ventilatorias y estructurales del sueño que aparecen en el SAOS, constituye la adenoamigdalectomia parcial, el tratamiento de elección que logra revertir las manifestaciones clínicas y polisomnográficas en la mayoría de los pacientes.